Cerdanyola del Vallès, 31 de octubre de 2018 Investigadores del Instituto de Biología Molecular de Barcelona (IBMB-CSIC) y del Instituto de Biotecnología y Biomedicina (IBB-UAB) han descubierto el mecanismo por el cual la bacteria Mycoplasma genitalium (Mge) se adhiere a las células humanas. Esta adhesión es esencial para el establecimiento de la infección y el posterior desarrollo de la enfermedad.
Mge es un patógeno emergente responsable de varias infecciones genitourinarias. En hombres, es una de las principales causas de uretritis (15-20%) y en mujeres, se ha asociado a cuadros de cervicitis, enfermedad inflamatoria pélvica, parto prematuro y aborto espontáneo. Hasta ahora se sabía que la adhesión de la bacteria al tracto genitourinario tiene lugar por medio de unas proteínas, denominadas adhesinas, que reconocen receptores específicos en la superficie de las células.
En este estudio, los investigadores del IBMB-CSIC han determinado la estructura tridimensional de la adhesina P110 de Mge unida a estos receptores celulares mediante difracción de rayos X con cristalografía de proteínas en la línea de luz XALOC. “Hemos hecho cristales que contenían la adhesina P110 unida al receptor y los hemos difractado con los rayos X del sincrotrón, lo que nos ha revelado la posición exacta de los átomos en la proteína y hemos podido definir la estructura en tres dimensiones”, explica David Aparicio, investigador del IBMB.
Paralelamente, científicos del IBB-UAB han realizado estudios in vivo con células humanas y han demostrado que mutaciones en lugares concretos de la proteína P110 impiden la unión de Mge. Estos resultados han permitido confirmar la información derivada de la estructura tridimensional obtenida.
Los resultados permiten entender las bases moleculares de la unión de Mge con las células humanas. “Por un lado, hemos conseguido información clave sobre el proceso de colonización, es decir, la toma de contacto del patógeno con las células del huésped. Por otro, esto nos permite desarrollar fármacos alternativos a los antibióticos capaces de bloquear la adhesión de Mge a las células, como moléculas que mimeticen los receptores celulares, o que estimulen la formación de anticuerpos que inhiban la función de las adhesinas”, explica Oscar Quijada, investigador del IBB.
La investigación ha propiciado la solicitud de una patente internacional y se ha iniciado una colaboración con el servicio y el grupo de investigación en microbiología del Campus Vall d’Hebron con el objetivo de luchar contra la aparición de resistencias.
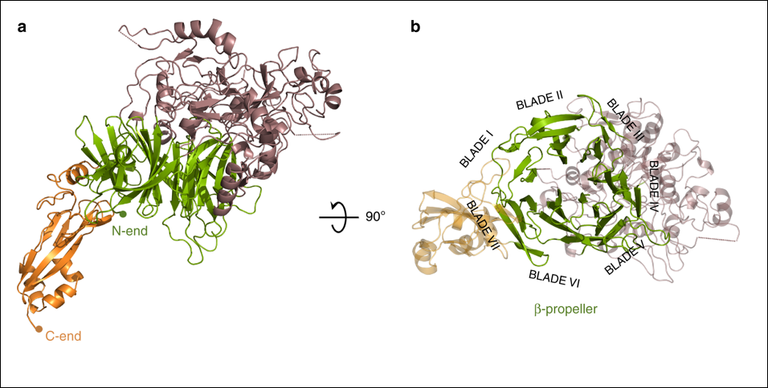
Estructura general de P110. Dos vistas, separadas 90º entre sí, de la región extracelular de P110 que está formada por un gran dominio N, con una hélice β de siete palas (verde), la corona (marrón) y el dominio C (naranja). En el panel lateral derecho, la vista es a lo largo del eje central de la hélice β. La situación de las siete palas en la hélice se indica explícitamente y muestra que las dos palas terminales I y VII están cerca del dominio C-terminal y opuestas a la corona. Imagen de Nature Communications, D. Aparicio, S. Torres-Puig, M. Ratera, E. Querol, J. Piñol, O.Q. Pich y I. Fita.
La resistencia a antibióticos
Actualmente, las infecciones de Mge son tan frecuentes como las de gonorrea, una de las infecciones de transmisión sexual más conocidas. Además, Mge se está convirtiendo en una superbacteria resistente a todos los antibióticos disponibles actualmente, hecho que pronto nos dejará sin alternativas terapéuticas. La resistencia a antibióticos es un problema cada vez más prevalente. Mediante cambios genéticos, muchas bacterias han desarrollado la capacidad de resistir a los antibióticos y continuar reproduciéndose. A pesar de que es un proceso natural, el mal uso y el abuso de estos medicamentos está acelerando el proceso. Dado que Mge está desarrollando resistencia a todos los antibióticos disponibles, hallar una estrategia terapéutica alternativa es especialmente relevante. Los resultados obtenidos son esenciales para el diseño de nuevos fármacos, puesto que permiten definir la adhesión a escala molecular.
Referencia: David Aparicio, Sergi Torres-Puig, Mercè Ratera, Enrique Querol, Jaume Piñol, Oscar Q. Pich, and Ignacio Fita. Mycoplasma genitalium adhesin P110 binds sialic-acid human receptors. Nature Communications. DOI 10.1038 / s41467-018-06963-i
Artículo original Universitat Autònoma de Barcelona




